氧化镁的结构示意图
想象你手中握着一块看似普通的白色粉末,它或许来自实验室的试剂瓶,或许藏匿于耐火材料的核心,又或许散落在医药产品的细微之处。这块看似不起眼的粉末,就是氧化镁,一种由镁和氧元素通过离子键紧密结合而成的化合物。它的化学式简单而纯粹——MgO,但在这简单的符号背后,隐藏着复杂的晶体结构和多样的物理化学性质。今天,就让我们一起深入探索氧化镁的结构示意图,揭开它神秘的面纱。
氧化镁的基本构成
氧化镁的结构示意图首先揭示了它最基本的构成单元——镁离子(Mg)和氧离子(O)。在化学反应中,镁原子倾向于失去两个外层电子,形成带两个正电荷的镁离子(Mg2?);而氧原子则倾向于获得两个电子,形成带两个负电荷的氧离子(O2?)。这两种离子通过强烈的静电吸引力相互结合,形成了稳定的离子化合物——氧化镁。
在氧化镁的晶体结构中,每个镁离子被六个氧离子所包围,形成八面体配位结构;反之,每个氧离子也被六个镁离子所包围。这种配位方式不仅体现了离子键的强度,也展示了氧化镁晶体的高对称性和规则性。想象这些离子像是在一个巨大的三维迷宫中,每个离子都精确地占据着特定的位置,共同构建出一个坚固而稳定的晶体框架。
氧化镁的晶体结构
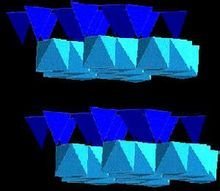
氧化镁的晶体结构属于立方晶系,空间群为Fm3m,晶格常数为4.212 ?。这种结构与我们熟悉的氯化钠(NaCl)非常相似,因此氧化镁也常被称为“立方氧化镁”。在氧化镁的结构示意图中,你可以清晰地看到每个镁离子和氧离子之间的距离,以及它们在空间中的排列方式。
这种立方晶系的结构赋予了氧化镁许多独特的物理性质。例如,由于离子键的强度和晶体结构的规整性,氧化镁具有极高的熔点(2852°C)和沸点(3600°C)。这意味着在极高的温度下,氧化镁仍然能够保持其稳定性,不会轻易分解或变形。这也是为什么氧化镁常被用作耐火材料和高温隔热材料的原因。
此外,氧化镁的密度为3.58 g/cm3,在室温下呈现出白色或米黄色的粉末状。这些物理性质不仅与其晶体结构密切相关,也决定了它在实际应用中的多样性和广泛性。
氧化镁的微观结构
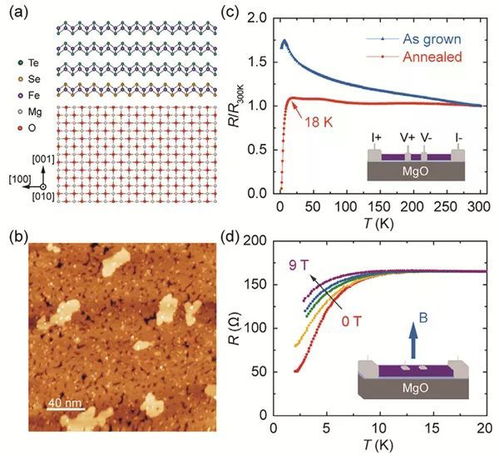
在微观层面,氧化镁的结构示意图还展示了其颗粒的形态和尺寸。未经过高温煅烧的氧化镁颗粒通常呈球状,且大小不均。经过高温煅烧(例如1500°C)后,这些颗粒会趋于均一化,表面变得更加致密光滑。
这种微观结构的变化对氧化镁的性质和应用产生了重要影响。例如,经过高温煅烧的氧化镁颗粒具有更高的密度和更小的比表面积,这使得它在某些应用中表现更加优异。例如,在医药领域,轻质氧化镁由于疏松多孔的结构,具有更好的吸附性能,可以用于制作胃药,帮助中和胃酸。
氧化镁的物理化学性质
氧化镁的物理化学性质与其晶体结构和离子构成密切相关。首先,作为碱性氧化物,氧化镁能够与酸发生反应,生成相应的镁盐和水。例如,当氧化镁与盐酸反应时,会生成氯化镁和水:
MgO + 2HCl → MgCl? + H?O
这种反应不仅体现了氧化镁的碱性,也展示了它在化学转化中的重要作用。
此外,氧化镁还具有良好的吸湿性。在空气中,氧化镁会吸收水分和二氧化碳,逐渐转化为碱式碳酸镁(MgCO·Mg(OH)·3H?O)。因此,在储存和使用氧化镁时,需要将其密封保存,以防止其吸湿变质。
氧化镁的应用领域
氧化镁的多样性质使其在许多领域都有广泛的应用。在工业领域,氧化镁是重要的耐火材料,常被用于制造耐火砖、耐火管和耐火坩埚等。由于氧化镁具有极高的熔点和良好的耐高温性能,它能够在高温环境下保持稳定,不会轻易熔化或变形。
在医药领域,氧化镁也是一种常见的药物成分。由于其碱性,氧化镁可以中和胃酸,缓解胃痛和胃灼热等症状。此外,氧化镁还具有吸附性能,可以用于吸附胃肠道中的有害物质,保护肠胃健康。
此外,氧化镁还广泛应用于建材、化工、电子等领域。例如,在建材领域,氧化镁可以用于制造防火墙、防火板等;在化工领域,氧化镁可以用于制造催化剂、吸附剂等;在电子领域,氧化镁可以用于制造绝缘材料、压电材料等。
通过深入探索氧化镁的结构示意图,我们



